COMO A ISOMERIA AFETA SEU COTIDIANO
- Principia Júnior

- 3 de ago. de 2021
- 3 min de leitura
Quantos objetos em pares você, leitor, possui em sua casa? Certamente um par de tênis, talvez um par de luvas também. Além de seus pertences, diversas moléculas também existem aos pares e se fazem tão presentes em nosso dia a dia quanto os calçados e meias que utilizamos.

Isomeria
Para entendermos o papel dessas moléculas em nossas vidas, precisamos entender breves conceitos de Química (Não se preocupe, são breves mesmo!).
Em Química, Isomeria é o estudo de diferentes moléculas de igual fórmula molecular. Na publicação anterior (A Química do Mel) são vistos dois isômeros de posição: a glicose e a frutose.
Estereoisomeria
E quando as moléculas têm igual conectividade entre os átomos? Então provavelmente elas se diferenciam pelo seu arranjo espacial. Portanto, estereoisômeros são moléculas iguais em conectividade entre os átomos, mas espacialmente diferentes.
Enantiômeros
Entre os estereoisômeros estão os enantiômeros, que são de nosso interesse nessa publicação. Tratam - se de isômeros espaciais, cujas moléculas são quirais, isto é, imagens especulares não sobreponíveis. Sendo assim, moléculas enantioméricas existem aos pares, tal qual nossas mãos.
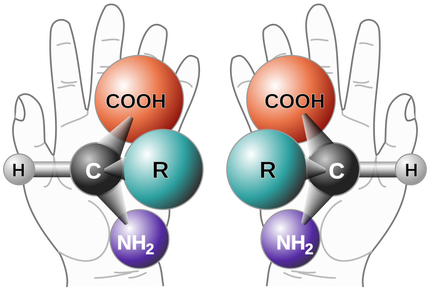
A nomenclatura dos enantiômeros obedece ao sistema "R e S", que faz referência a cada carbono assimétrico presente na estrutura.
Os enantiômeros apresentam várias propriedades físicas semelhantes, tais como ponto de fusão e ebulição, solubilidade em solventes, densidade, entre outras. A única diferença está na direção que um feixe de luz polarizado é desviado. Um dos enantiômeros vai desviar a luz para a direita, e o outro para a esquerda.
Por conta disso, esses compostos também são nomeados como isômeros ópticos, e é comum que sejam nomeados também de acordo com o desvio da luz polarizada. Aquele que desvia para direita é representado por "D" (Destrógiro) ou "+", e aquele que desvia para a esquerda é identificado por "L" (Levógiro) ou "-".
Essas pequenas diferenças estruturais e ópticas são capazes de afetar nosso cotidiano, desde o aroma que sentimos até os efeitos de um medicamento. Separamos aqui alguns exemplos:

Aromas
Um clássico exemplo está no odor da laranja e do limão. Ambos se devem ao par de isômeros do Limoneno. O R - Limoneno corresponde ao odor da laranja, e o S - Limoneno é responsável pelo odor do limão.
Portanto, é possível afirmar que as narinas do ser humano são aceptores estereoespecíficos!
Farmoquímica
Muitos fármacos são compostos enantioméricos. Um dos enantiômeros apresenta as propriedades de interesse. Por sua vez, sua imagem especular pode ser inativa, fracamente ativa ou, na pior das hipóteses, danosa ao ser humano.
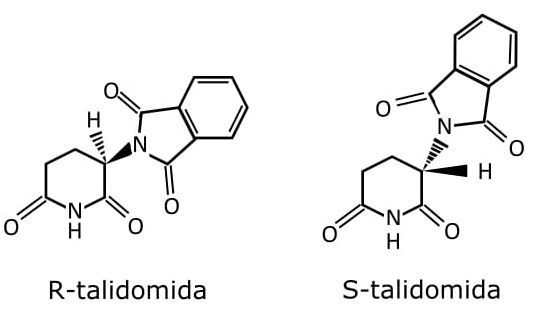
É o famoso e trágico caso da talidomida. A R-(+)-Talidomida apresenta propriedades sedativas, interessantes para gestantes, mas a S-(-)-Talidomida tem efeitos teratogênicos. Em condições fisiológicas, este par se interconverte, o que comprometeu o desenvolvimento de muitas crianças pós gestação. Após o evento (este fármaco foi comercializado em mais de 140 países), concentrou-se muita atenção por parte da comunidade científica para o emprego dos isômeros ópticos
Lateralidade da Vida
19 dos 20 aminoácidos essenciais (A Valina é destacada a seguir) que compõem todas as proteínas conhecidas são quirais. Contudo, para cada aminoácido, apenas o enantiômero “L” (levógiro) deriva dos animais e plantas. O porquê dessa preferência natural é tema de debates científicos e filosóficos com respeito a origem da vida.

Em resumo, a isomeria contempla nossa vida em diversos objetos, alimentos e fármacos. Poderia-se citar mais exemplos (vitamina C, hormônios, etc). Como viu-se, a Isomeria está presente desde o surgimento da vida que conhecemos e é um traço marcante na Química e em nosso cotidiano. Incrível como moléculas tão semelhantes podem ter funções e aplicabilidades tão distintas, não é mesmo?
Referências
SOLOMONS, T. W. G.; FRYHLE, C. B. Química Orgânica, 10ª edição, LTC – Livros Técnicos e Científicos Editora S. A ., Rio de Janeiro, 2012, p. 189-198.
OLIVEIRA, L. A.; QUADROS, A. L. O Uso do Caso Talidomida Auxiliando na Construção de Significados em Aulas de Química do Ensino Superior. Química Nova, v. 43, n. 4, 2020, p. 486-492. Disponível em: <https://doi.org/10.21577/0100-4042.20170487>.
Tabela de aminoácidos. Disponível em: <http://www.fcfar.unesp.br/alimentos/bioquimica/imagens/TABELA_AA.GIF>.




Comentários